����(ri)������(li)��㷢������ƣ���˾���뾳������й�Ʊ��H�ɣ��������������������������(le)�½�(jin)չ(zhan)����˾��(yi)��2024��7��10��(ri)������������ݽ���(le)���η��е����룬����ͬ��(ri)�������������վ������(le)���η��е���������(liao)��
�Ӱ���(li)��㵱ǰ���о��뿪�������з���������Ҫ�۽���ADC������ż��ҩ���˫��/���(deng)�ؼ�������з��ϡ�ͬʱ����˾��HER3��һ�е��(jin)����(le)�ص�Ͷ�룬����(li)����HER3/EGFR˫��ADCҩ��BL-B01D1����ҵ�ڹ�ע��
�ڴ�(ci)֮ǰ����ʱ��ʩ�����¼�ơ�BMS������(yi)�����(li)����BL-B01D1ҩ����ȫ��ս�Ժ���(zuo)Э�飬��Э���漰�ߴ�8����Ԫ������ܶ�84����Ԫ�ĺ���(zuo)�������Э�����BMS��(yi)�ڱ����֧����(le)8����Ԫ��Ԥ�����

��Ȼ����HER3������ҩ����ҵ�ھ߱��㷺�Ͽɵ���ҵ��ֵ��Ȼ����HER3�е㷢������δ(wei)�����еij�ҩ���֣����ҩ���з���������(lie)������6�£�Ĭɳ���͵�һ��(san)���з���ȫ����HER3 ADCҩ��Patritumab Deruxtecan���ڵ���(san)������ԭ(yuan)��(yin)��FDA������ʳƷҩƷ�ල����(li)�֣��ӳ�������(bu)�����з���(jin)�����������ڰ���(li)�����BL-B01D1ҩ�
��(yin)��(ci)������(li)�����BL-B01D1ҩ���з�����ҵ������Ľ�(jin)չ(zhan)��������ҵ���������ƶ����������Ե���Ҫ���塣ͬʱ�����ܰ���(li)�����(yi)���BMS 8����ԪԤ�������BL-B01D1δ(wei)�����ٴ��о�����ҵ�ƹ���(reng)��������ʽ�Ͷ����ȷ����˳��(li)��(jin)�С�
�з�����ҵ����BL-B01D1ҩ����з���ս
��������(liao)��ʾ������(li)�����(zi)1996�괴��������������(le)����ҩ������ҩת�䡣����(li)�����Ҫ�۽���ADC������ż��ҩ���˫��/���(deng)�ؼ�������з��ϣ���2014����������ͼ������(le)SystImmune������ʼ(shi)�з�first-in-class��EGFR��HER3˫��ADC (BL-B01D1)��
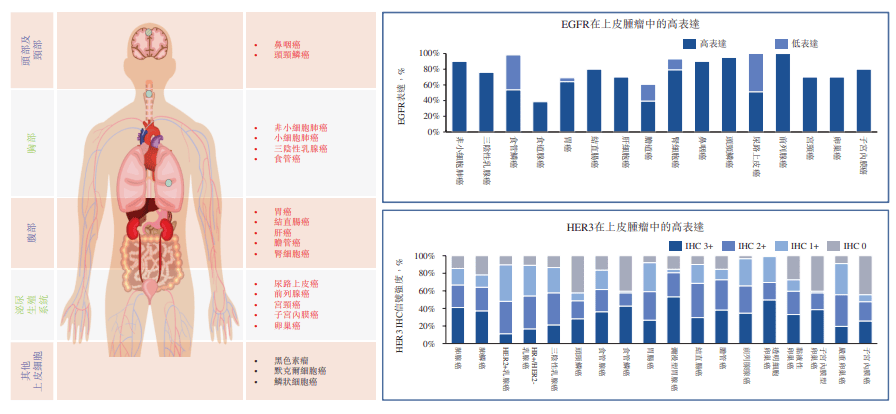
����(le)�⣬BL-B01D1��һ�����EGFR��HER3˫�е�Ŀ���ż��ҩ�ADC����EGFR��HER3����ƤԴ�������г�(cheng)�ֳ��㷺�Ҹ߱�������ԡ�ͨ����˫���ṹ��BL-B01D1�ܹ��㷺�ذ������ʵ���������Ҹ��Ӹ�����������֯���Ӷ���ǿ����ɱ�˻��ԡ����ٰж��ԣ��ڶ�����������(liao)�����ž���ٴ�����ҵ��ֵ��
BL-B01D1ҩ����(zuo)ΪӰ�����(li)����ֵ�ĺ���Ҫ��(su)�����з���̬ʼ(shi)��Ϊҵ������ע����2023��12�£�����(li)�����BMS��(jiu)BL-B01D1ҩ������(le)ȫ��ս�����ɼ�����(zuo)���ף������ܶ�ߴ�84����������������Ϊ8������
��(ci)��ײ�(bu)��ˢ����(le)ȫ��ADC�����е�һ�ʲ�������ʷ��¼���������(li)���ʵ����(le)��(cai)��Ť��Ϊӯ����(zi)�յ�8��������������(li)���ɹ���2023��ĩ(mo)�Ŀ���״(zhuang)̬ŤתΪ2024��һ��(ji)��ĩ(mo)��ӯ��(li)״(zhuang)̬����ӯ��(li)��ߴ�50�ڡ�
����BL-B01D1ҩ���з���(jin)չ(zhan)�����������з���������(reng)���ٽϸߵķ���(xian)����(zi)1989�귢��HER3�е�������(yi)����30�꣬��2008�����HER3�е����(liao)����(jin)����(le)�ٴ�����Σ�Ȼ�����ڽ���������Լ����ڼ�ø���Լ��͵�(deng)��ս��HER3�İ���ҩ���з�һֱδ(wei)��ȡ��ʵ��(zhi)��ͻ�ƣ�����(zhi)������δ(wei)���κ����HER3�İ���ҩ������������
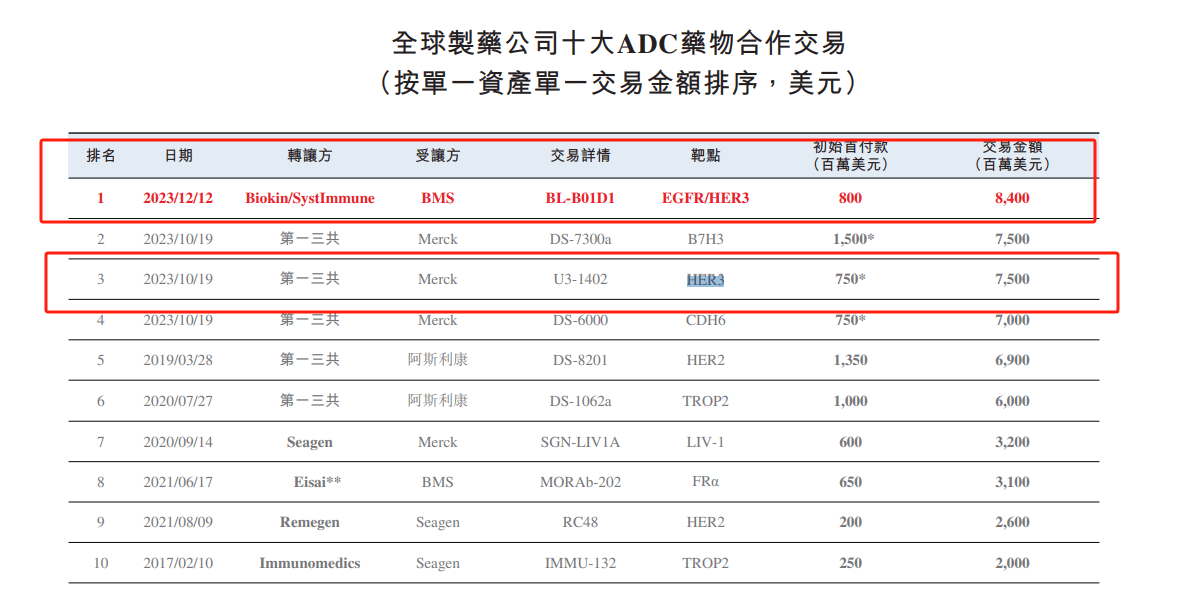
���������(liao)��ʾ����ȫ��ʮ(shi)��ADCҩ�����(zuo)�����У�������(liang)��ҩ��۽���HER3�е㡣���У�����(le)����(li)����BL-B01D1ҩ���⣬Ĭɳ�����һ��(san)�������з���Patritumab Deruxtecan���о���(jin)����ΪѸ�١�Ȼ����Patritumab Deruxtecan�ڽ���6����(yin)����(san)���������������FDA���ӳ�����
ֵ�ù�ע���ǣ������(li)���BL-B01D1ҩ����ȣ�ɳ�����һ��(san)�������з���Patritumab Deruxtecanҩ���з���(jin)����������(xian)������FDA��Patritumab Deruxtecanҩ��������������ӳ٣����ǣ�������ܻ�����δ(wei)�Ը�ҩ��İ�(an)ȫ�Ժ���Ч������κ���(zhi)�ɡ���(liang)�ҹ�˾�����������ĺ������ύ�˲����룬�Խ�(jin)һ���ƶ�ҩ������н�(jin)�̡�
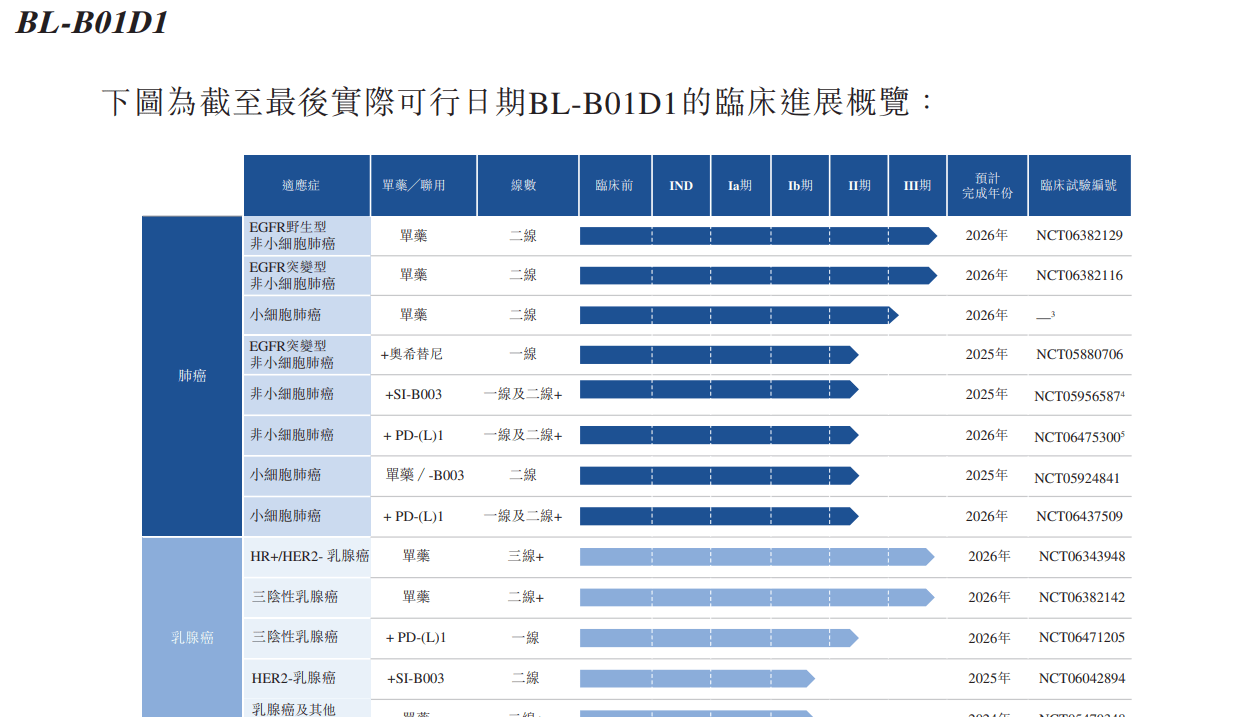
���۰���(li)���BL-B01D1ҩ��ڷΰ������ٰ���θ�������ж���ڢ����ٴ���II���ٴ�������(ta)��֢(zheng)����(reng)�Ƣ�/����̽�����ٴ��Σ�����ҩ��Ԥ����(wan)�������2025-2026���ڼ䡣������(lu)��ҩҵ������(shen)�����̵ĸ����ԣ���ҩ������ʵ����ҵ����ʱ�佫��Ϊ������
���й�˵��(ming)�����(xian)��ʾ�У�����(li)���Ҳ��ʾ������˾��ҵ��ǰ���ںܴ�̶���ȡ���ں�ѡҩ�����BL-B01D1���ijɹ����ȹ�˾��(wu)���ɹ���(wan)��ҩ����ٴ���������ü������ʵ����ҵ������˾�ڽ�(jin)�������κ�����ʱ�����ش������ɱ���֧����˾��ҵ��ǰ�����ܻ��ܵ��ش�(bu)��(li)Ӱ�졣ͬʱ����˾���ټ���(lie)���������������ֿ��ܱȹ�˾�������ɹ��ط��֡���������ҵ������ҩ���
�����߰�(ang)���ó����ǣ�Ԥ��������ȷ�ϴ�����
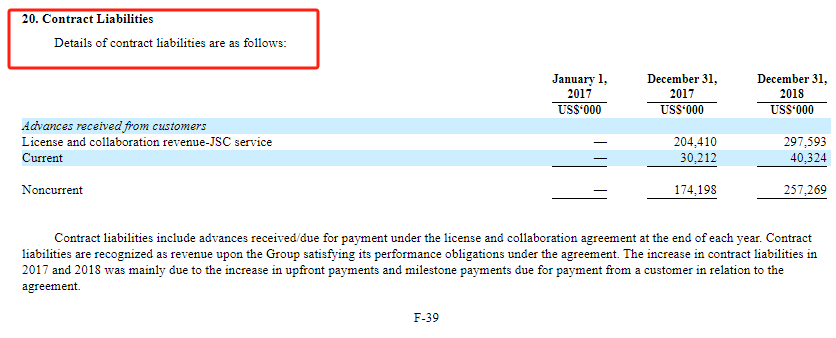
������BMSǩ����غ���(zuo)Э�飬�ڽ���һ��(ji)�Ȱ���(li)���ɹ����յ�BMS֧����8����ԪԤ�������(bu)�������ڸñ�Ԥ�������(li)���ֱ��ȷ��Ϊ���룬����(zhi)һ��(ji)�ȵİ���(li)������(li)��������������BMS�����(cai)���У����ñʡ����ñ�עΪ����(li)����ӹ�˾SystImmune��Ԥ���
��Ԥ����ȷ��Ϊ���룬�ܵ�Ͷ������(zhi)�ɡ�����(li)����α�ʾ������(jie)��2024��3��7��(ri)����˾��(yi)�յ���BMS֧����8����Ԫ������ݺ���(zuo)Э��Լ(yue)������˾Ӧ��BMS��(shou)��BL-B01D1��ص�֪ʶ��Ȩ�Ķ������ɣ���(jie)��2024��3��31��(ri)����˾������(shou)Ȩ������(lu)Լ(yue)��ʵ�������2024���һ��(ji)��ȷ����(le)�����(shou)Ȩ�������룬���ϻ�������ع涨����
ֵ�ù�ע���ǣ�����(li)�����BMS�Ľ���ģʽ����(bu)������һ��(ban)���ԣ�ҩ������(shou)�����й������ȫ��Ȩ�棬����Ŀ�չ(zhan)�ٴ����з��ķ����ɹ������е���������(li)�����BMS��ͬ�ֵ�BL-B01D1ȫ�����ã��Լ��������г�����(li)��Ϳ������������й���½���⣬����(li)��㽫�Ӿ����۶�����ȡ�ּ�����Ȩʹ�÷ѡ�
��ʵ�ϣ�����(li)�����BMS�ĺ���(zuo)ʵ������һ�ֹ�ͬ�����ɷ֣������ض�������ʵʩȨ��ת�á�����˫����ǩ���Э�����BMS�����й���½�ľ����۶��л������Ȩʹ�÷ѡ����������й���½���⣬����(li)����ȫ���ӹ�˾SystImmune���Ӿ����۶�����ȡ�ּ�����Ȩʹ�÷ѡ���(ci)����ζ�ţ�����BL-B01D1ҩ������Ȩ�棬����(li)��㽫��(bu)�����ж�������Ȩ��������BMS�����(li)��㹲�С�
����(li)���Ķ��³������ڹ���������Ҳ��ʾ�������ǰ���(li)���ĵ�һ�ʲ��Ǵ����ת�ý��ף�����һ�ֺ���(zuo)��������ҵ���Ļ���ϵ����
���ֺ���(zuo)������һ���汣����(le)���Ȩ�棬�������(le)ҩ���з��ɹ����Զ�����档������һ���棬����ģʽҲ���ٺܴ�ˣ�����(li)�����Ҫ�е��߶�ĺ����з����ٴ����ã��Լ�����DZ�ڵ��ٴ�ʧ�ܷ���(xian)��
���ݹ�����ʾ������(li)��㽫�ֵ�BL-B01D1������������(gan)�������á���(li)��������ζ�ţ�BL-B01D1���ڿ����У�����(li)�����Ҫ�е��߶���ٴ��������á�BMS�����(li)���Ԥ����8����Ԫ����Լ�Ԥ�ڵ�5����Ԫ�������Ҫ���ں����ٴ�������(deng)���á�
���й�˵��(ming)���У�����(li)���Ҳ��ʾ�������Ǵ���ҩ������е�ҩ���δ(wei)�����κ�˾��Ȩ�����С������ܹ��Ӳ�Ʒ�����в����κ�����֮ǰ�����ǵĹ��߲�Ʒ������Ҫ������ٴ�ǰ���u���ٴ�������������Լ���Ͷ�ʼ�����Ӫ������(zuo)����
ֵ�ù�ע���ǣ�����(li)��㹲ͬ��������(zuo)ģʽ��ҵ������(xian)����ѭ��������(zhang)����(li)�ϣ�����(li)���ȴ����ҵ��������(an)�����ڲ�(cha)�졣��2017�괫������ɹ��Ƴ�������CAR-T��(liao)����ƷΪ�����ù�˾��ǿ��ǩ����(le)��ͬ�ƽ�(jin)�ٴ���������ҵ����Э�飬ǿ��Ϊ��(ci)֧����(le)�ߴ�3.5����Ԫ�Ĵ���¼���
Ȼ���������(li)��㲻(bu)ͬ���������ﲢδ(wei)��ǿ��֧�����������ֱ��ȷ��Ϊ���룬����ѡ����ȷ��Ϊ��ͬ��ծ���������ļ����У�����(zhao)��ͬ�������ʱ�����ȷ��Ϊ���롣
������ʿָ������Ȼ����(li)���ǿ��(diao)������Э�����BMS��˾֧����8����Ԫ�����������(zhi)Ϊ��(bu)���˻�����(bu)�ɵֿ�(kou)�����ǣ���ȫ�濼������Э���ܵı����£���8����Ԫ����Ӧ��������84����Ԫ��Э���ܶ��(hu)��������ͬ����������(bu)Ӧ��(zuo)Ϊ�����������(jin)��ȷ�ϡ�
�ڷ���(xian)��ʾ�У�����(li)����ʾ����BMS���ܲ�(bu)�ᰴ�ƻ���(lu)�����������ܾܾ���(lu)������BMSЭ���µij�ŵ��BMSδ(wei)��(lu)Լ(yue)��������ֹBMSЭ���������(wu)����ɫ���µĻ��������(zuo)��飬�����ܶ����ǵ����뼰�з�������ʽ��������Ӱ�졣��